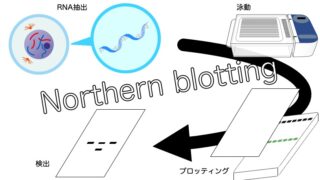
【保存版】生命科学系の実験で使用する溶液やバッファーを調製する方法
記事内に商品プロモーションを含む場合があります
生命科学系の実験で使用する溶液やバッファーの調製方法をまとめています。
モル濃度計算機を作成しました。
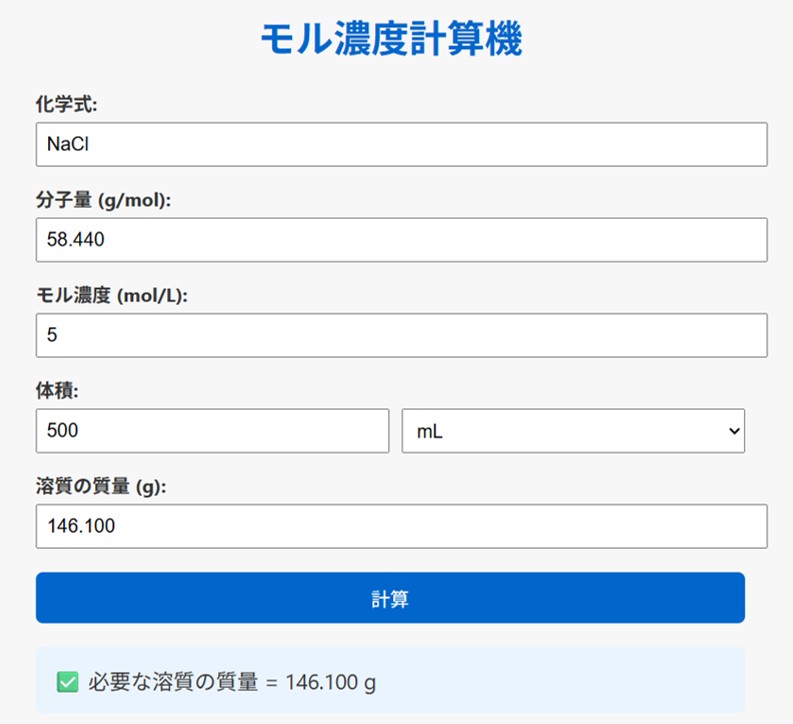
ご利用はコチラから
Contents
一般的なストック溶液
10M 酢酸アンモニウム
核酸のエタノール沈殿に、よく使用される。特に、dNTPや糖類、30mer程度のプライマーの共沈を軽減する目的で使用される。
作り方(1リットル)
- 770.8gの酢酸アンモニウムを800mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
- オートクレーブで滅菌し、室温で保存する。
1M 塩化カルシウム
作り方(1リットル)
- 219.08gの塩化カルシウム六水和物を800mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
- オートクレーブで滅菌し、室温で保存する。
250×デンハート液(デンハルト液)
ノーザンブロット法およびサザンブロット法、in vitroでのDNA-DNA(もしくはRNA)交雑実験において、非特異的な会合や吸着を抑制する、ブロッキング剤として用いられる。
組成
- 5% Ficoll 400
- 5% ポリビニルピロヒドン(PVP)
- 5% ウシ血清アルブミン(BSA)
作り方(1リットル)
- 50gのFicoll 400、50gのPVP、50gのBSAを600mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
- 25mlずつに小分け分注し、冷凍保存する。
3M 酢酸ナトリウム
核酸のエタノール沈殿に、よく使用される。エタノール沈殿で最も一般的に使用され、最終濃度0.3Mになるように添加する。pH5.2はRNA用、pH7.0はDNA用とするプロトコールもあるが、DNAにpH5.2を用いても問題ない。
作り方(1リットル)
- 408.24gの酢酸ナトリウム三水和物を800mlの精製水に溶解させる。
- 氷酢酸でpH5.2に、または希酢酸でpH7.0に調整する。
- 精製水で1リットルにメスアップする。
- オートクレーブで滅菌し、室温で保存する。
1M DTT
作り方(20ml)
- 3.085gのDTTを20mlの10mM酢酸ナトリウム(pH5.2)に溶解させる。
- 0.22µmフィルターで濾過滅菌する。
- 1mlずつに小分け分注し、冷凍保存する。
0.5M EDTA(pH8.0)
作り方(1リットル)
- 186.12gのNa2EDTA-2H2Oを800mlの水に溶解させる。
- pHを測定しながらNaOH(20gほど)を添加して、pH8.0に調整する。
- 精製水で1リットルにメスアップする。
- オートクレーブで滅菌し、室温で保存する。
0.1M IPTG
作り方(50ml)
- 1.19gのIPTGを40mlの精製水に溶解させる。
- 精製水で50mlにメスアップする。
- 0.22µmフィルターで濾過滅菌する。
- 5mlずつに小分け分注し、冷凍保存する。
1M MgCl2
作り方(1リットル)
- 203.31gの塩化マグネシウム六水和物を800mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
- オートクレーブで滅菌し、室温で保存する。
5M NaCl
作り方(1リットル)
- 292.2gの塩化ナトリウムを800mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
- オートクレーブで滅菌し、室温で保存する。
10%SDS
作り方(1リットル)
- 100gのSDSを900mlの精製水に溶解させる。
- 68℃まで加熱し、結晶を溶解させる。
- 数十µl程度のHClでpH7.2に調整する。
- 精製水で1リットルにメスアップする。
- 室温で保存する。
100(w/v)% TCA
500gのトリクロロ酢酸を227mlの精製水に加えると、100%(w/v)TCAとなる。
20mg/ml X-gal
作り方(20ml)
- 400mgのX-galを20mlのN,N’-ジメチルホルムアミドに溶解させる。
- 500µlずつに、遮光されたガラスチューブもしくはポリプロピレンチューブへ分注し、冷凍保存する。
バッファー(緩衝液)
1M Tris
作り方(1リットル)
- 122.14gのトリスを800mlの精製水に溶解させる。
- pHを測定しながらHClを添加して(下表参考)、目的のpHに調整する。
- 精製水で1リットルにメスアップする。
| 目的とするpH | 加えるHCl(原液)の目安量(ml) |
|---|---|
| 6.8 | 79 |
| 7.0 | 77 |
| 7.4 | 69 |
| 7.6 | 63 |
| 8.0 | 46 |
| 8.8 | 13 |
10×MOPS
作り方(1リットル)
- 41.85gのMOPSと6.80gの酢酸ナトリウム三水和物を800mlのDEPC処理水に溶解させる。
- 20mlのDEPC処理0.5M EDTA溶液を加え、10M NaOhでpH7.0に調整する。
- DEPC処理水で1リットルにメスアップする。
- 冷蔵かつ遮光状態で保存する。
10×PBS
作り方(1リットル)
- 80gのNaCl、2gのKCl、26.8gのNa2HPO4-H2O、2.4gのKH2PO4を800mlの精製水に溶解させる。
- HClでpH7.4に調整する。
- 精製水で1リットルにメスアップする。
- オートクレーブで滅菌し、室温で保存する。
20×SSC
作り方(1リットル)
- 175.3gのNaCl、88.2gのクエン酸ナトリウム二水和物を800mlの精製水に溶解させる。
- HClでpH7.0に調整する。
- 精製水で1リットルにメスアップする。
- オートクレーブで滅菌し、室温で保存する。
20×SSPE
作り方(1リットル)
- 175.3gのNaCl、27.6gのNaH2PO4-H2O、7.4gのNa2EDTAを800mlの精製水に溶解させる。
- 数ml程度の10M NaOH溶液でpH7.4に調整する。
- 精製水で1リットルにメスアップする。
- オートクレーブで滅菌し、室温で保存する。
1×TE
組成
- 10mM Tris
- 1mM or 0.1mM EDTA
作り方(1リットル)
- 10mlの1M Tris(pH8.0〜7.4)、2mlもしくは200µlの0.5M EDTA(pH8.0)を800mlの精製水に添加する。
- 混合し、精製水で1リットルにメスアップする。
- オートクレーブで滅菌し、室温で保存する。
0.1M 酢酸ナトリウム
0.1M 酢酸(1リットル)
- 5.78mlの氷酢酸を500mlの精製水と混合する。
- 精製水で1リットルにメスアップする。
0.1M 酢酸ナトリウム(1リットル)
- 13.605gの酢酸ナトリウム三水和物を800mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
0.1M 酢酸ナトリウム緩衝液の作り方(100ml)
下表を参考に、0.1M 酢酸・0.1M 酢酸ナトリウムを混合する。
| 目的のpH | 0.1M 酢酸(ml) | 0.1M 酢酸ナトリウム(ml) |
|---|---|---|
| 3.6 | 90.1 | 9.9 |
| 3.8 | 85.2 | 14.8 |
| 4.0 | 78.4 | 21.6 |
| 4.2 | 69.6 | 30.4 |
| 4.4 | 59.1 | 40.9 |
| 4.6 | 47.7 | 52.3 |
| 4.8 | 36.5 | 63.5 |
| 5.0 | 26.6 | 73.4 |
| 5.2 | 18.6 | 81.4 |
| 5.4 | 12.6 | 87.4 |
| 5.6 | 8.4 | 91.6 |
0.1M 酢酸カリウム
0.1M 酢酸(1リットル)
- 5.78mlの氷酢酸を500mlの精製水と混合する。
- 精製水で1リットルにメスアップする。
0.1M 酢酸カリウム(1リットル)
- 9.814gの酢酸カリウムを800mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
0.1M 酢酸カリウム緩衝液の作り方(100ml)
下表を参考に、0.1M 酢酸・0.1M 酢酸カリウムを混合する。
| 目的のpH | 0.1M 酢酸(ml) | 0.1M 酢酸カリウム(ml) |
|---|---|---|
| 3.6 | 90.1 | 9.9 |
| 3.8 | 85.2 | 14.8 |
| 4.0 | 78.4 | 21.6 |
| 4.2 | 69.6 | 30.4 |
| 4.4 | 59.1 | 40.9 |
| 4.6 | 47.7 | 52.3 |
| 4.8 | 36.5 | 63.5 |
| 5.0 | 26.6 | 73.4 |
| 5.2 | 18.6 | 81.4 |
| 5.4 | 12.6 | 87.4 |
| 5.6 | 8.4 | 91.6 |
0.1M リン酸ナトリウム
0.1M リン酸二水素ナトリウム(1リットル)
- 15.601gのNaH2PO4-2H20を500mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
0.1M リン酸水素二ナトリウム(1リットル)
- 26.807gのNa2HPO4-7H2Oを500mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
0.1M リン酸ナトリウム緩衝液の作り方(100ml)
下表を参考に、0.1M リン酸二水素ナトリウム・0.1M リン酸水素二ナトリウムを混合する。
| 目的のpH | リン酸二水素ナトリウム(ml) | リン酸水素二ナトリウム(ml) |
|---|---|---|
| 5.7 | 96.9 | 3.1 |
| 5.8 | 96.2 | 3.8 |
| 5.9 | 95.2 | 4.8 |
| 6.0 | 94.1 | 5.9 |
| 6.1 | 92.6 | 7.4 |
| 6.2 | 90.9 | 9.1 |
| 6.3 | 88.8 | 11.2 |
| 6.4 | 86.3 | 13.7 |
| 6.5 | 83.4 | 16.6 |
| 6.6 | 79.9 | 20.1 |
| 6.7 | 76.0 | 24.0 |
| 6.8 | 71.5 | 28.5 |
| 6.9 | 66.6 | 33.4 |
| 7.0 | 61.3 | 38.7 |
| 7.1 | 55.7 | 44.3 |
| 7.2 | 50.0 | 50.0 |
| 7.3 | 44.3 | 55.7 |
| 7.4 | 38.7 | 61.3 |
| 7.5 | 33.4 | 66.6 |
| 7.6 | 28.5 | 71.5 |
| 7.7 | 24.0 | 76.0 |
| 7.8 | 20.1 | 79.9 |
| 7.9 | 16.6 | 83.4 |
| 8.0 | 13.7 | 86.3 |
0.1M リン酸カリウム
0.1M リン酸二水素カリウム(1リットル)
- 13.609gのKH2PO4を500mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
0.1M リン酸水素二カリウム(1リットル)
- 17.418gのK2HPO4を500mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
0.1M リン酸カリウム緩衝液の作り方(100ml)
下表を参考に、0.1M リン酸二水素カリウム・0.1M リン酸水素二カリウムを混合する。
| 目的のpH | リン酸二水素カリウム(ml) | リン酸水素二カリウム(ml) |
|---|---|---|
| 5.7 | 96.9 | 3.1 |
| 5.8 | 96.2 | 3.8 |
| 5.9 | 95.2 | 4.8 |
| 6.0 | 94.1 | 5.9 |
| 6.1 | 92.6 | 7.4 |
| 6.2 | 90.9 | 9.1 |
| 6.3 | 88.8 | 11.2 |
| 6.4 | 86.3 | 13.7 |
| 6.5 | 83.4 | 16.6 |
| 6.6 | 79.9 | 20.1 |
| 6.7 | 76.0 | 24.0 |
| 6.8 | 71.5 | 28.5 |
| 6.9 | 66.6 | 33.4 |
| 7.0 | 61.3 | 38.7 |
| 7.1 | 55.7 | 44.3 |
| 7.2 | 50.0 | 50.0 |
| 7.3 | 44.3 | 55.7 |
| 7.4 | 38.7 | 61.3 |
| 7.5 | 33.4 | 66.6 |
| 7.6 | 28.5 | 71.5 |
| 7.7 | 24.0 | 76.0 |
| 7.8 | 20.1 | 79.9 |
| 7.9 | 16.6 | 83.4 |
| 8.0 | 13.7 | 86.3 |
DNAの電気泳動で使用するバッファー

10×DNAローディングバッファー
作り方(100ml)
- 250mgのブロモフェノールブルーおよび/または250mgのキシレンシアノールを33mlの150mM Tris(pH7.6)に溶解させる。
- 60mlのグリセロールと7mlの精製水を混和する。
- 室温で保存する。
50×TAE
作り方(1リットル)
- 242gのTrisを500mlの精製水に溶解させる。
- 100mlの0.5M EDTA(pH8.0)と57.1mlの氷酢酸を添加する。
- 精製水で1リットルにメスアップする。
- 室温で保存する。
10×TBE
作り方(1リットル)
- 108gのTris、55gのホウ酸を900mlの精製水に溶解させる。
- 40mlの0.5M EDTA(pH8.0)を添加し、精製水で1リットルにメスアップする。
- 室温で保存する。
10mg/ml エチジウムブロマイド
作り方(100ml)
- 1gのエチジウムブロマイドを100mlの精製水に添加する。
- 完全に溶けるまで攪拌する。
- 冷蔵かつ暗所で保存する。

DNA・RNAをアガロースゲルで電気泳動する原理・方法を解説!よくある失敗の原因3選も DNAやRNAを電気泳動することができるみたいだけど、原理がよくわかっていない なぜ核酸が動いていくの?分かれていくの? ...
RNA実験に使用する試薬
溶液のDEPC処理
RNAを分解する酵素であるRNaseを失活させるために、RNA実験で使用する溶液はDEPC(ジエチルピロカーボネート、Diethylpyrocatbonate)で処理する。
- 計量した溶液を試薬ビンに入れる。
- DEPCを0.1%加えて激しく振り混ぜ、完全に混和する。
- ドラフト内でオーバーナイトでインキュベートする。
- オートクレーブし、残留DEPCを不活性化する。
- 室温で保存する。
2×RNAローディングバッファー(変性ゲル用)
RNAサンプルに対して等量加えてよく混合し、70℃で10分間加熱する。その後氷上で1分間急冷してスピンダウンした後、変性ゲルへアプライする。
組成
- 95(v/v)% 脱イオンホルムアミド
- 0.025(w/v)% SDS
- 0.025(w/v)% ブロモフェノールブルー
- 0.025(w/v)% キシレンシアノール
- 0.5mM EDTA
作り方(100ml)
- 95mlの脱イオンホルムアミド、25mgのSDS、25mgのブロモフェノールブルー、25mgのキシレンシアノール、100µlの0.5M EDTA(pH8.0)を混合する。
- 1mlずつに小分け分注して、冷凍保存する。
タンパク質の電気泳動(SDS-PAGE)に用いる溶液


10% 過硫酸アンモニウム(APS)
作り方(10ml)
- 1gの過硫酸アンモニウム(APS)を8mlの精製水に溶解させる。
- 精製水で10mlにメスアップする。
30(w/v)% アクリル-ビスアクリル-アミド混合液
作り方(100ml)
- 29gのアクリルアミドと1gのN,N’-メチレンビスアクリルアミドを60mlの精製水に溶解させる。
- 溶液を37℃まで加熱して試薬を溶解させる。
- 精製水で100mlにメスアップする。
- 冷蔵かつ遮光状態で保存する。
1.5M Tris-HCl(pH8.8)
作り方(1リットル)
- 181.71gのトリスを約800mLの精製水に溶解する。
- pHを測定しながらHClを添加して(約20.1mL)、目的のpHに調整する。
- 精製水で1リットルにメスアップする。
0.5M Tris-HCl(pH6.8)
作り方(1リットル)
- 60.57gのトリスを約800mLの精製水に溶解する。
- pHを測定しながらHClを添加して(約39.8mL)、目的のpHに調整する。
- 精製水で1リットルにメスアップする。
5×SDS-PAGEサンプルバッファー
組成
- 250mM Tris(pH6.8)
- 50(v/v)% グリセロール
- 5(w/v)% SDS
- 0.08(w/v)% ブロモフェノールブルー
作り方(100ml)
- 50mlの0.5M Tris-HCl(pH6.8)に5gのSDSおよび80mgのブロモフェノールブルーを溶解させる。
- 50mlのグリセロールを添加し、よく混和する。
10×SDS-PAGE泳動バッファー
作り方(1リットル)
- 10gのSDS、30.3gのTris、144.1gのグリシンを800mlの精製水に溶解させる。
- 精製水で1リットルにメスアップする。
CBB染色液
作り方(1リットル)
- 2.5gのCoomassie Brilliant Blue R-250を、450mlのメタノール、100mlの酢酸、400mlの精製水の混合液に溶解させる。
- 精製水で1リットルにメスアップする。
CBB脱色液
作り方(1リットル)
- 450mlのメタノール、100mlの酢酸、400mlの精製水を混合する。
- 水で1リットルにメスアップする。



【SDS-PAGE】タンパク質を分子量で分ける原理から失敗例まで解説! ※本ページにはプロモーションが含まれます SDS-PAGEでなぜタンパク質を分離することができるの? SDS-PAGE...
ウェスタンブロッティングで用いる溶液


1×転写バッファー
作り方(1リットル)
- 2.9gのグリシン、5.8gのTris、0.37gのSDSを200mlのメタノールに溶解させる。
- 精製水で1リットルにメスアップする。
ポンソーS溶液
作り方(100ml)
- 2gのポンソーS、30gのトリクロロ酢酸、30gのスルホサリチル酸を80mlの精製水に溶解させる。
- 精製水で100mlにメスアップする。
20×TBS(pH7.4)
組成
- 1M Tris
- 3M NaCl
作り方(1リットル)
- 121.14gのTris、175.32gのNaClを800mlの精製水に溶解させる。
- HClでpH7.4に調整する。
- 精製水で1リットルにメスアップする。
1×TBS-T
組成
- 50mM Tris
- 150mM NaCl
- 0.1(v/v)% Tween20
作り方(1リットル)
- 50mlの20×TBSに1mlのTween20を溶解させる。
- 精製水で1リットルにメスアップする。



ウェスタンブロッティング(WB)でタンパク質を検出・定量する原理を解説!失敗の原因まで! 皆さんはウェスタンブロッティング(Western blotting)、ウェスタンブロット(Western blot)について説明できま...
ABOUT ME